Genom-Editierung beim Rind: aktueller Stand
Die Genom-Editierung (engl.: Genome Editing) ist ein neues Biotechnologie-Tool, das erhebliche Chancen und Herausforderungen in der Züchtungsforschung beinhaltet. Es ermöglicht eine präzise Genomänderung, indem DNA-Sequenzen effizient und genau eingeführt, gelöscht oder ersetzt werden. Diese Modifikationen können Phänotypen (= spezifische Merkmale) gezielt verändern und so den Zuchtprozess beschleunigen.
Die Genom-Editierung wird zwischenzeitlich für Veränderungen sowohl von Genomen interessierender Mikroorganismen (= weiße Gentechnik) als auch von Pflanzen (= grüne Gentechnik), Tieren (= rote Gentechnik) bzw. beim Menschen (= Gentherapie) genutzt. Im Rahmen einer Genom-Editierung werden sogenannte Designer-Endonukleasen (Genscheren) eingesetzt (Abb. 1). Diese Enzyme schneiden doppelsträngige DNA an einer vorbestimmten Zielsequenz. Es entstehen somit Doppelstrangbrüche. Diese Doppelstrangbrüche können einerseits der DNA-Reparatur oder andererseits dem Einfügen (‚Knockin‘) oder Ausschalten (‚Knockout‘) spezifischer DNA-Sequenzen dienen (Abb. 1).
Abb. 1: Schematische Darstellung von Genome Editing (eigene Grafik)
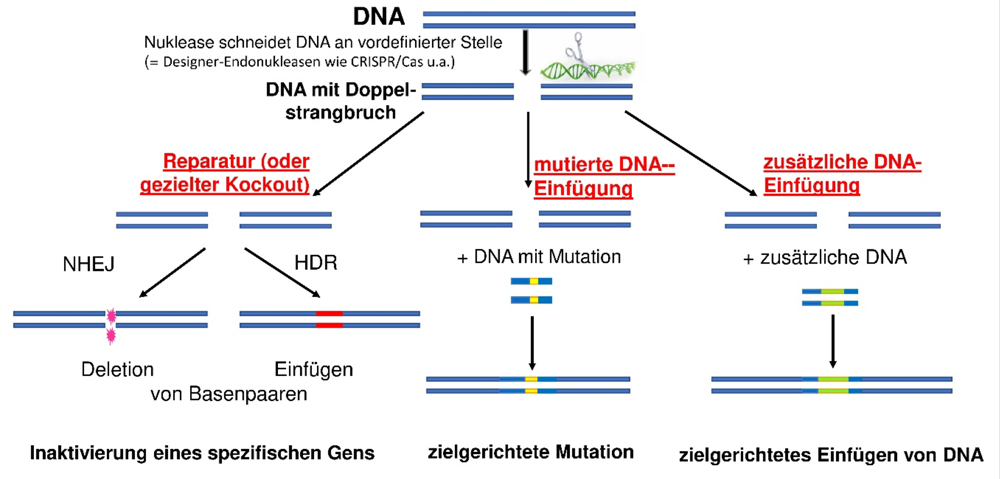
Anm.: Designer-Endonuklease = ‚Genschere‘ bestehend aus zwei funktionellen Bereichen (= gewünschte Stelle im Genom erkennen und DNA an der richtigen Stelle schneiden); NHEJ = nicht-homologe Reparatur (engl.: non-homologous end-joining); Deletion = ‚Löschen‘ (oder Zerstören) einer Nukleotidsequenz oder eines Teils der Nukleotidsequenz; homologe Reparatur = engl.: homology directed repair (HDR)
Während die spezifische Erkennung der interessierenden DNA-Region bei der sogenannten TALEN-Methodik auf einen bestimmten Proteinteil beruht, wird bei der CRISPR/Cas-Technik die vorbestimmte (Ziel-)DNA-Region durch eine RNA vermittelt (Larson et al., 2013, Brade, 2019, Xu et al., 2025).
Das CRISPR/Cas-System
Die bahnbrechende CRISPR/Cas-Methode wurde maßgeblich von Emmanuelle Charpentier und Jennifer Doudna entwickelt. Die Genom-Editierung umfasst bei Nutzung des CRISPR/Cas-System (= Genschere) drei Schritte:
- Finden: Der CRISPR-Abschnitt erkennt mit Hilfe der darin integrierten RNA (= Guide RNA) das jeweilige Ziel; eine bestimmte Sequenz in der umzuschreibenden Ziel-DNA.
- Schneiden: Das an den CRISPR-Abschnitt gekoppelte Cas-Protein schneidet den DNA-Doppelstrang genau an der gewünschten Zielsequenz. Beide Elemente (CRISPR bzw. Cas) werden synthetisch hergestellt. Sie müssen dann in die Ziel-Zelle eingeführt werden.
- Reparieren/DNA-Modifizieren: Die zelleigenen Reparatursysteme fügen den durchtrennten DNA-Strang wieder zusammen. Je nachdem, wie das geschieht, können einzelne DNA-Bausteine entfernt oder modifiziert werden. Möglich ist auch, kurze DNA-Sequenzen neu einzubauen.
Genom-Editierung verringert vor allem solche Probleme, die aus den Zufälligkeiten bisheriger Techniken (beispielsweise der früheren Mutationszüchtung) erwuchsen.
In praxi bedeutet das: Zeit- und Kostenersparnis. Bis dato sind in der EU noch keine Genom-Editierung-Tiere zugelassen, anders in den USA oder Brasilien, wo bereits erste Genom-Editierung-Rinder eine Marktzulassung erhalten haben (Van Eenennaam et al., 2021; Hock, 2024).
Aktueller Stand der Genom-Editierung bei Nutzpflanzen
Die Nutzung der Genom-Editierung ist in der grünen Gentechnik gegenüber der roten Gentechnik vergleichsweise weit fortgeschritten. Die Möglichkeiten zur gezielten Nutzung der Genom-Editierung-Technik sind hier vielfältig:
- Gene ausschalten:
- Man kann beispielsweise gezielt ein interessierendes Gen ausschalten. Das macht nicht nur in der Grundlagenforschung Sinn, sondern auch, um Gene für unerwünschte Proteine (Stoffe) zu deaktivieren (z.B. Allergene).
- Inaktive Gene wieder aktivieren:
- Mit Genom-Editierung könnten die Folgen spezifischer Mutationen „rückgängig“ gemacht und betreffende Gene wieder aktiviert werden.
- Neue Strategien im Pflanzenschutz:
- Viele Erreger von Krankheiten (Viren, Bakterien etc.) sind außerordentlich anpassungsfähig. Mit Genom-Editierung können die Genetiker im Wettlauf mit den Erregern gewissermaßen Zeit gewinnen und schneller zu gewünschten Resistenzen kommen.
- Spezifische Gene in das Genom neu einführen:
- Spezifische Zuchtziele realisieren.
Im März 2025 wurde eine neue Verordnung für Genom-Editierungsanwendungen bei Pflanzen mit qualifizierter Mehrheit vom Rat der EU angenommen. Damit konnte das übliche Trilog-Verfahren zwischen Kommission, EU-Parlament und Rat mit dem Ziel beginnen, in Zukunft eine neue EU-Verordnung für Genom-Editierung-Pflanzen zu etablieren.
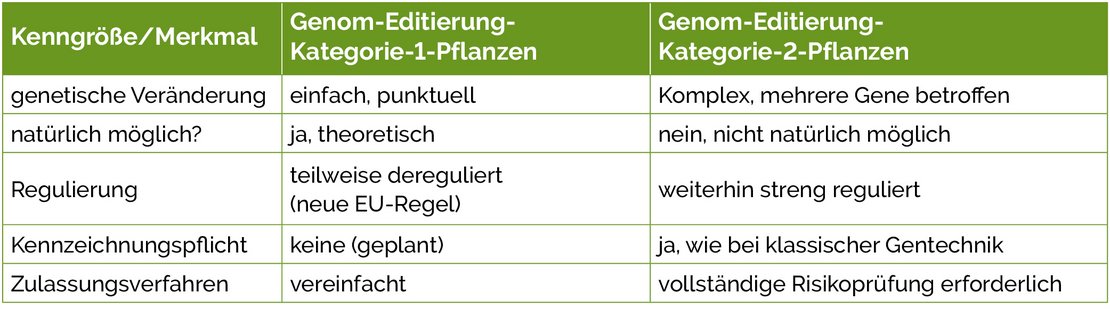
Zu ergänzen bleibt, dass im aktuellen EU-Verordnungsvorschlag zugehörige Pflanzen zwei Genom-Editierungskategorien zugeordnet werden (vgl. auch Tab. 1):
- Genom-Editierung-Kategorie-1-Pflanzen: Diese Pflanzen werden punktuell und präzise genetisch verändert, z. B. für Krankheitsresistenz oder bessere Anpassung an extreme Wetterbedingungen. Sie könnten theoretisch auch natürlich entstehen und gelten als risikoarm. Beispiele sind:
- Salat, der langsamer braun wird
- Tomaten mit blutdrucksenkender Wirkung
- Genom-Editierung-Kategorie-2-Pflanzen: Diese Pflanzen wurden komplexer verändert als Genom-Editierung-Kategorie-1-Pflanzen. Sie fallen weiterhin unter das klassische Gentechnikrecht der EU und unterliegen strengen Vorschriften.
Die Rinderzüchtung wird sich weiterentwickeln. Dies eröffnet neue Möglichkeiten aber beinhaltet auch neue Risiken. Die Zukunft bleibt herausfordernd und gleichzeitig spannend (Foto. W. Brade)

Tab. 1: Charakterisierung von Genom-Editierung-Kategorie-2-Pflanzen gegenüber Genom-Editierung-Kategorie-1-Pflanzen
Bleibt die Frage zu beantworten, ob Genom-editierte Lebensmittelprodukte bereits in der EU für den Handel zugelassen sind?
Die Antwort lautet: nein!
Eine Zulassung Genom-editierter Lebensmittelprodukte hängt u.a. von der finalen Verabschiedung der oben genannten neuen Genom-Editierungsverordnung ab, die derzeit noch verhandelt wird (für weitere Details siehe auch BfR, 2025).
Nutzung gentechnisch veränderter Futtermittel in der Rinderfütterung
Der Großteil des Futters, das in Deutschland an Rinder verfüttert wird, ist ‚gentechnikfrei‘. Es stammt von unseren Feldern, auf denen bereits seit 2012 keine gentechnisch veränderten Pflanzen mehr angebaut werden dürfen. Mit anderen Worten: deutscher Mais oder Soja sind gentechnikfrei.
Dennoch erhalten viele Nutztiere in Deutschland Futter, das zumindest teilweise aus gentechnisch veränderten Pflanzen (= GV-Pflanzen) erzeugt wurde.
In Deutschland werden zwar keine GV-Pflanzen angebaut, aber importierter GV-Mais und vor allem -Soja sind ein zentraler Bestandteil unserer Tierfütterung
‚Importiertes‘ Soja‘ ist überwiegend gentechnisch verändert, da ein Großteil des Welthandels mit Sojabohnen bzw. -schrot aus Ländern wie Brasilien und den USA erfolgt, in denen fast nur noch GV-Sojabohnen angebaut werden.
Die aktuelle Kritik an diesen Importen bezieht sich dabei allerdings nicht nur auf den Anbau von GV-Pflanzen, sondern auch auf die zugehörigen Anbaubedingungen in solchen Herkunftsländern wie Brasilien oder Argentinien; die meist wenig nachhaltig sind (Monokulturen, hoher Pestizideinsatz, Waldrodung etc.).
Anzumerken bleibt an dieser Stelle, dass GV-Futtermittel in der EU gekennzeichnet werden müssen. Das gilt auch für Mischfutter und für Futtermittelbestandteile (BZL, 2024).
Anders als die Futtermittel selbst müssen jedoch die damit erzeugten Lebensmittel nach dem europäischen Lebensmittelrecht nicht gekennzeichnet werden.
Die Verbraucher können somit nicht erkennen, ob tierische Produkte wie Milch oder Fleisch von Tieren stammen, die mit GV-Futtermitteln gefüttert wurden. Wenn keine derartigen Futtermittel eingesetzt worden sind, können Hersteller dies jedoch auf freiwilliger Basis durch die Verwendung der ‚Ohne Gentechnik‘-Kennzeichnung für interessierte Verbraucher sichtbar machen (BZL, 2024).
Laut Europäische Behörde für Lebensmittelsicherheit (EFSA) wirken sich gentechnisch veränderte Futtermittel - nach heutigem Stand der Forschung - nicht auf Milch oder Fleisch der Tiere aus.
Erinnert werden muss an dieser Stelle daran, dass verzehrte Proteine im Tierkörper in der Regel bis zu ihren Bestandteilen (Aminosäuren) zerlegt werden (Flachowsky et al., 2017; Brade, 2019; Caradus, 2023). Deshalb wird es seitens der EFSA als äußerst unwahrscheinlich eingeschätzt, dass gentechnisch veränderte Futterbestandteile, wie DNA oder Proteine, die in den Körper der Tiere übergehen, dazu führen, dass Resistenzen übertragen oder Allergien ausgelöst werden können (vgl. auch EFSA, 2023).
Aktuelle Gen-Editing-Projekte beim Rind
Die Ziele in der roten Gentechnik sind im Großen und Ganzen ähnlich derjenigen in der grünen Gentechnik; ‚nur‘ spezifiziert für das Tier.
In erster Linie geht es somit darum, Gesundheit und Wohlergehen der Nutztiere zu fördern sowie die Produktivität zu steigern.
Weltweit nutzen immer mehr Forschergruppen die Genom-Editierungstechnik; auch im Bereich der Rinderzucht. In mehreren Projekten sind bereits lebende Rinder mit veränderten Eigenschaften erzeugt worden; andere befinden sich noch in frühen Forschungsstadien. Einige interessante Beispiele sind in Tabelle 1 zusammengestellt.
Tab. 1: Realisierte Genom-Editierungsprojekte beim Rind (Beispiele)
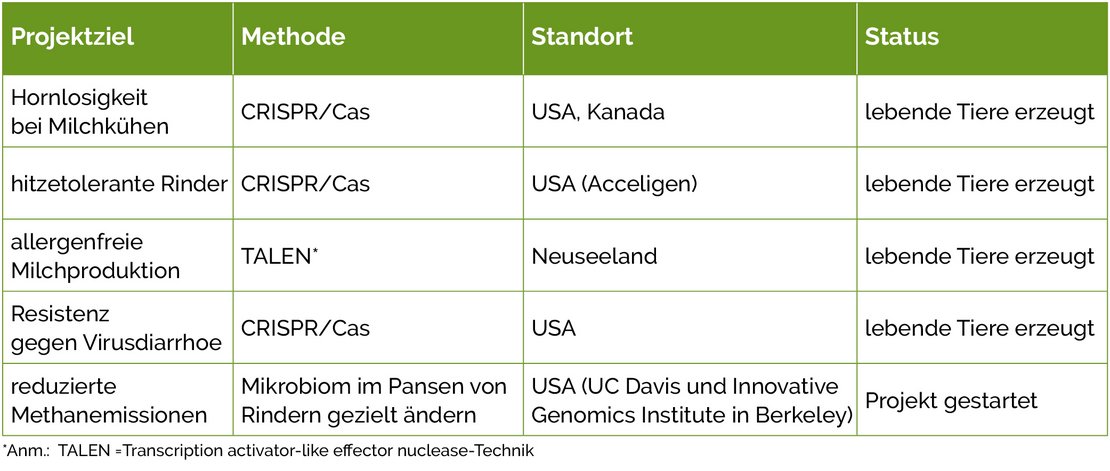
Nachfolgend werden einige Studien mit Genom-Editierung beim Rind detaillierter aufgezeigt.
Genom-Editierung-Hornlos-Rinder (GE-Polled-cattle) mit unbeabsichtigten DNA-Veränderungen
Nur noch wenige Milcherzeuger halten heutzutage Rinder mit Hörnern. Um die Verletzungs- und Unfallgefahr zu minimieren, werden die Tiere kurz nach der Geburt ‚künstlich‘ enthornt. Das Problem: trotz Betäubung und Schmerzmittelgabe ist die Enthornungsprozedur für die Kälber mit Schmerzen und Tierleid verbunden. Studien deuten sogar darauf hin, dass die Tiere noch Monate später schon bei leichter Berührung Schmerzreaktionen zeigen. Die ‚Hornlos-Zucht‘ erspart somit die Enthornungs-Prozedur bei Kälbern und damit Tierleid (Brade, 2020, 2022).
Das Start-up-Unternehmen ‚Recombinetics‘ (St. Paul, USA) machte sich durch ein frühes Genom-Editierungsprojekt zur Entwicklung von hornlosen Rindern einen Namen. Die 2015 geborenen, ersten gentechnisch erzeugten hornlosen Rinder wurden leider auch zu „Genom-Editierungs-Berühmtheiten“.
In der Zeitschrift ‚Nature Biotechnology‘ berichteten Carlson et al. (2016) von Recombinetics stolz, dass es keine unerwarteten Veränderungen, wie unerwünschte DNA-Insertionen oder -Deletionen als Ergebnis ihres Geneditierungsverfahrens gab. Doch spätere DNA-Analysen der US-Food and Drug Administration (FDA) zeigten, dass die Genome der beiden Kälber unbeabsichtigte DNA-Veränderungen enthielten (versehentlich eingeführte Bakterien-DNA wurden in der Nähe der DNA-Schnittstelle nachgewiesen – vgl. auch Norris et al., 2019).
Solche sogenannten Off-Target-Effekte entstehen, wenn die eingesetzten Gen-Scheren nicht nur an der gewünschten Zielsequenz schneiden, sondern beispielsweise auch an ähnlichen, aber nicht identischen DNA-Stellen.
Die Wissenschaftsgemeinschaft hat zwischenzeitlich die potenziellen Gefahren von Off-Target-Effekte erkannt.
Obwohl das CRISPR/Cas-Werkzeug im Vergleich zu anderen (bisherigen) Gentechniken relativ zuverlässig eine anvisierte Erbgutsequenz erkennt und schneidet, sind leider „DNA-Fehlschnitte“ nicht völlig ausgeschlossen. So können „ungeplante“ Mutationen im Genom entstehen, die es zu verhindern gilt.
Anzumerken bleibt allerdings auch, dass solche Off-Target-Effekte mithilfe von
DNA-Screeningverfahren leicht identifiziert und damit solche Tiere beispielsweise von der weiteren Zuchtverwendung ausgeschlossen werden können (Van Eenennaam, 2019, Young et al., 2020).
Mittels Genom-Editierung erzeugte Rinder mit verändertem Prolaktin-Rezeptor
(‚PRLR-SLICK-Rinder‘)
Ein Gen, das nachweislich verschiedene Mutationen aufweist und eine Variation bezüglich der Thermotoleranz bei Rindern bedingt, ist der Prolaktin-Rezeptor (Littlejohn et al., 2014, Cuellar et al, 2024).
Bisher wurden insgesamt sechs separate Einzelnukleotid-Polymorphismen (SNP) im Prolaktin-Rezeptor bei Rinderrassen identifiziert, die vorrangig in der Karibik entstanden sind. Diese Mutationen werden auch als SLICK-Genvarianten bezeichnet, da Tiere, die entweder ein oder zwei Kopien dieser Mutation erben, ein glattes, kurzes Haarfell aufweisen (Dikmen et al., 2014).
Eine Funktion von Prolaktin besteht darin, das Haarwachstum zu hemmen so dass ‚glatte‘ Rinder (‚SLICK-Rinder‘, engl. ‚slick‘; dtsch.: glatt) entstehen (Abb. 2).
Abb. 2: Beispiel für Unterschiede im zugehörigen Phänotyp.

Der ca. einjährige Angus-Bulle, der eine Gen-editierte PRLR-Variante (links mit der Ohrmarke: S013) trägt, hat ein sehr kurzes Haarkleid, das typisch für SLICK-Tiere ist. Dies lässt sich durch einen zugehörigen Vergleich mit einem Nicht-Gen- editierten Tier (Ohrmarke S010) - vor allem im Kopf- und Nackenbereich – gut dokumentieren. Zu beachten ist auch das stärkere Auftreten von Falten bei dem PRLR-SLICK Tier (Fotomontage des Autors).
Mithilfe der CRISPR/Cas-Technik gelang es, eine gezielte genomische Veränderung am Prolaktinrezeptor-Gen (PRLR) einzuführen und so PRLR-SLICK-Rinder zu erzeugen.
Im März 2022 veröffentlichte die US-amerikanische Food and Drug Administration (FDA) eine Risikobewertung des von Acceligen™ eingereichten Antrags bezüglich dieser Genom-Editierung- Rinder. Die FDA stufte die Veränderung als „risikoarm“ ein (FDA, 2022). Es war damit das erste Mal, dass die FDA Genom-Editierung-Rinder für die Lebensmittelproduktion in den USA zuließ.
Weitere (spätere) Auswertungen (im August 2022 in Florida; USA) beinhalteten eine detaillierte Bewertung der PRLP-SLICK-Tiere unter Hitzestressbedingungen (Abb. 3).
Abb. 3: Unterschiede zwischen SLICK- und Nicht-SLICK-Tieren bei der Regulierung der Körpertemperatur unter Hitzestressbedingungen (im August 2022) in Florida (eigene Grafik in Anlehnung an Cuellar et al., 2024)
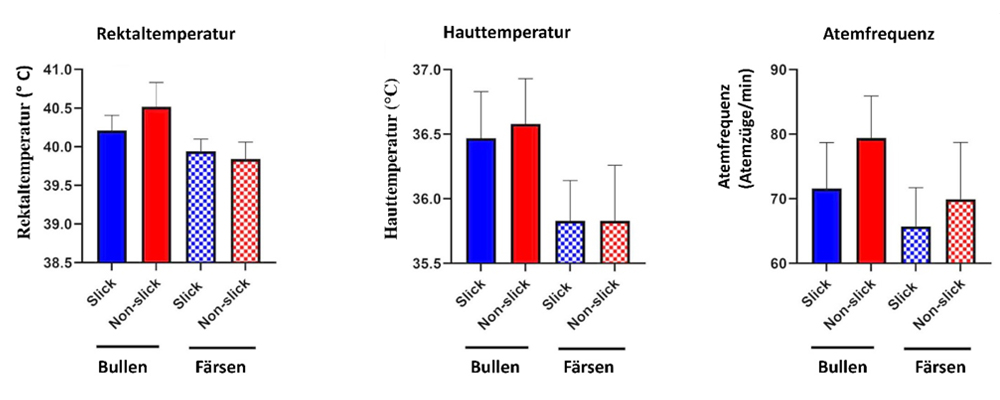
Die rektale Temperatur war für (männliche) PRLP-SLICK-Tiere – unter Hitzestressbedingungen – tendenziell niedriger. Zusätzlich zeigten die PRLP-SLICK-Tiere auch in der Atemfrequenz gewisse Vorteile (Cuellar et al., 2024).
Es gab keinen Unterschied im Geburtsgewicht der ‚glatten‘ im Vergleich zu den ‚nicht-glatten‘ Tieren. Darüber hinaus konnten keine negativen Folgen in der Fortpflanzungsleistung der männlichen SLICK-Tiere beobachtet werden (Cuellar et al., 2024).
Mittels Genom-Editierung könnte somit die Einführung dieser Mutation in hochleistende Milchrinderrassen (zukünftig) weiter beschleunigt werden, sodass Kosten und Zeit – gegenüber einem alternativen (konventionellen) Ein- und Rückkreuzungsverfahren – gespart werden dürften (Cuellar et al., 2024).
Erzeugung eines CD46-editierten Kalbes
Das Bovine Virusdiarrhoe-Virus (BVDV) beeinträchtigt die Gesundheit und das Wohlbefinden von Rindern weltweit. Der wichtigste Wirtsrezeptor, der die BVDV-Infektion vermittelt, ist CD46. Ein Team aus mehreren staatlichen US-Forschungseinrichtungen und privatwirtschaftlich organisierten Firmen um Aspen Workman sowie Tad Sonstegard nutzten die CRISPR-vermittelte Genom-Editierung einschließlich des somatischen Zellkerntransfers, um ein lebendes Rind mit einem Austausch von sechs Aminosäuren in der BVDV-Bindungsdomäne des bovinen CD46-Gens zu erzeugen (Workman et al., 2023).
Das Ergebnis war ein Genom-Editierungskalb mit deutlich reduzierter Infektionsanfälligkeit. Auch wies dieses Kalb keine Off-Target-Editierungen auf.
Dieses präzisionsgezüchtete ‚Proof-of-Concept-Tier‘ lieferte den Beweis dafür, dass gezielte Genomveränderungen im CD46-Gen die Belastung durch BVDV-assoziierte Erkrankungen bei Rindern reduzieren können.
Die Autoren betonen jedoch auch, dass weitere Studien mit CD46-editierten Tieren erforderlich bleiben (Workman et al., 2023).
Erstellung von Beta-Lactoglobulin-Knockout-Kälbern
Etwa 3 % aller Säuglinge und Kleinkinder leiden in Westeuropa an einer Kuhmilchallergie, wobei Beta-Lactoglobulin eines der Hauptallergene ist. Durch die Entfernung von Beta-Lactoglobulin aus Kuhmilch könnte deren allergenes Potenzial verringert werden, so dass Kuhmilch eine wertvolle Nahrungsquelle auch für Kinder darstellen könnte, die derzeit (aufgrund von allergischen Reaktionen gegen Beta-Lactoglobulin keine Kuhmilch trinken können.
Ein neuseeländisches Team nutzte die Genom-Editierung zwecks Erzeugung von Beta-Lactoglobulin-Knockout-Kälbern erfolgreich (Wie et al., 2018).
Drei Rinder (zwei männliche und ein weibliches) wurden mit der gewünschten Deletion erzeugt. Obwohl die Mutation künstlich erzeugt wurde, ahmte sie eine natürliche Mutation (= Deletion) eines (kleinen) DNA-Abschnitts nach.
Die weitere Analyse der Milchzusammensetzung ergab einen leicht erhöhten Proteingehalt und einen niedrigeren Laktosegehalt. Beta-Lactoglobulin konnte in der Milchprobe nicht nachgewiesen werden. Kritisch anzumerken bleibt jedoch, dass die Milchanalyse nur anhand eines einzelnen Tieres möglich war.
Die Studie belegt(e) die mögliche Erzeugung präzise editierter Rinder zur sicheren Produktion hypoallergener Milch.
Nutzung der Genom-Editierung zur Manipulation ausgewählter mikrobieller Konsortien im Pansen von Rindern
Angesichts zunehmender klimabedingter Herausforderungen könnte sich die Technologie der Genom-Editierung auch als möglicher ‚Verbündeter‘ bzgl. einer emissionsarmen Rinderzucht erweisen.
Ein zentrales Ziel aktueller Studien bei Wiederkäuern ist die Reduktion von Methanemissionen durch gezielte Eingriffe in die methanogenen Archaeen-Populationen im Pansen.
In einer neuen Studie, veröffentlicht in der Zeitschrift ‚Science‘, nutzte ein interdisziplinäres Team aus Molekularbiologen und Geochemikern CRISPR/Cas, um die Aktivität des Enzyms Methyl-Coenzym-M-Reduktase (MCR) in Methanogenen gezielt zu verändern. Dieses Enzym spielt eine Schlüsselrolle bei der Methanproduktion.
Durch eine Reduzierung der Enzymaktivität konnten die Forscher beobachten, wie Methanogene auf Veränderungen in ihrer Nahrungsversorgung reagieren (Gropp et al., 2025).
Außerdem konnten die Autoren zeigen, dass nicht nur die Art der „Nahrung“ der Mikroben – wie Acetat oder Methanol – die Methanbildung bestimmt, sondern auch die Umweltbedingungen und die biochemischen Reaktionen der Mikroben selbst. So veränderten die Mikroben bei geringerer Enzymaktivität ihre Stoffwechselprozesse, was zu einer stärkeren Einbindung von Wasserstoff führte (Gropp et al., 2025).
Die direkte Anwendung von Genom-Editierung im Pansen zwecks Manipulation ausgewählter mikrobieller Konsortien im Pansen von Rindern ist allerdings damit noch nicht in praxi realisiert.
Es handelt sich um (erste) In-vitro-Studien oder ‚Proof-of-Concept‘-Experimente (= Machbarkeitsstudien); ein erster Einstieg zur Manipulation des Pansenmikrobioms von Wiederkäuern.
Diskussion
Herkömmliche Zuchtmethoden sind die Eckpfeiler in der aktuellen Rinderzüchtung. Sie umfassen eine selektive Zuchtarbeit (in Reinzucht und/oder in Kreuzungen) – aufbauend auf einer qualifizierten Zuchttierbewertung (= Zuchtwertschätzung) – sowie gezielten Anpaarungsstrategien und schließen assistierte Fortpflanzungstechniken (wie Embryotransfer und künstliche Besamung) konsequent ein.
In den letzten Jahren haben enorme Fortschritte in der Genomsequenzierung bzw. Genotypisierung von Zuchttieren zusätzlich eine kommerzielle Nutzung der genomischen Selektion in Rinderzuchtprogrammen ermöglicht.
Ein hervorragendes Beispiel ist die Umsetzung der genomischen Selektion bei Holstein-Rindern in den Vereinigten Staaten bzw. in zahlreichen westeuropäischen Staaten (Wiggans et al., 2022). Die gezielte Integration der genomischen Selektion hat nachweislich auch zu einem verbesserten genetischen Fortschritt in der deutschen Holsteinzucht geführt (Brade, 2023 a,b).
Genom-Editierung ist das neueste Werkzeug in Zuchtprogrammen. Mittels dieser Technik sind hochspezialisierte Genetiker in der Lage, die Rate der genetischen Verbesserung – speziell auch für Merkmale der Gesundheit und des Wohlbefindens – weiter zu beschleunigen.
Genom-Editierung ermöglicht – wie am Beispiel der PRLP-SLICK-Tiere in den USA oder der ß-LG-Knockout-Rinder in Neuseeland eindrucksvoll gezeigt wurde – die gezielte Etablierung wertvoller (neuer) Gene (Mutationen) oder ein ‚Abschalten‘ spezifischer DNA-Sequenzen innerhalb einer einzigen Generation.
Die weitere Kommerzialisierung dieses neuen Biotechnologie-Tools hängt allerdings auch von den sich schnell weiterentwickelnden Regulierungsgesetzen zur Risikobewertung von Genom-Editierungstieren ab, bei denen einige Länder (z.B. USA) bereits die Kommerzialisierung von Genom-Editierungsrindern bzw. deren Produkte erlaub(t)en.
Der zugehörige regulatorische Prozess ist jedoch auch dort weiter komplex. So verlangt das US-Landwirtschaftsministerium (USDA) weiterhin eine Überwachung transgener Organismen, denen fremde DNA zugeführt wird. Dies kann die kommerzielle Freigabe solcher Produkte von Genom-Editierungsorganismen verlangsamen oder erschweren. Darüber hinaus müssen sich die Unternehmen durch das komplexe Netz laufender Patentstreitigkeiten ‚kämpfen‘, insbesondere zwischen dem Broad Institute und der University of California. Diese Rechtsstreitigkeiten um Eigentum und Rechte beispielsweise an der CRISPR/Cas-Technologie haben weitreichende Auswirkungen und erhöhen oft die Komplexität und Kosten solcher Entwicklungsprozesse (o.V., 2025).
Genom-Editierung bietet somit Lösungen, die einst unerreichbar schienen. Die zugehörigen ethisch-moralischen Bedenken, beispielsweise bei der Erzeugung von Genom-Editierungsrindern, sind jedoch sehr vielfältig und betreffen sowohl das Tierwohl als auch gesellschaftliche, ökologische oder wirtschaftliche Fragen (Hock, 2024). Zu nennen sind diesbezüglich beispielsweise folgende Aspekte:
- Tierwohl und unvorhersehbare Folgen
Beispiel: ungewollte Mutationen. Auch bei präziser Genom-Editierung können unbeabsichtigte Veränderungen auftreten, die das Tier krank machen oder sein Verhalten verändern.
- Menschliche Kontrolle über Tiere
Die Vorstellung, Tiere nach menschlichen Wünschen zu formen, wirft Fragen nach moralischen Grenzen auf.
- Ökologische Risiken
Es besteht die Sorge, dass sich Genom-Editierungstiere ungewollt verbreiten.
- Transparenz und Kennzeichnung
Viele Verbraucher möchten keine Lebensmittel von Genom-Editierungstieren verzehren. Ohne klare Kommunikation könnten Verbraucher das Vertrauen in Landwirtschaft und Forschung verlieren.
- Monopolisierung der Züchtung
Große Biotech-Firmen könnten sich Patente sichern und damit die Pflanzen- und/oder Tierzucht weltweit dominieren.
Diese Bedenken führ(t)en dazu, dass die Genom-Editierung – besonders in (West-)Europa – sehr kontrovers diskutiert wird. Manche sehen darin eine Chance für eine nachhaltigere Landwirtschaft, andere warnen vor einer vielschichtigen Grauzone.
Die Technik der Genom-Editierung ist nicht per se gefährlich. Sie ist ein Werkzeug, mit dem verantwortungsvoll umgegangen werden muss. Dazu sind Regeln notwendig.
Die Erhaltung der biologischen Vielfalt, Vermeidung einer Gesundheitsgefährdung bei Menschen und Tieren sowie der Schutz von Umwelt und Boden sollten immer mitberücksichtigt werden. Die wiederholt angemahnte Vorsicht verantwortungsvoller Forscher bei Anwendung/Nutzung der Genom-Editierung ist deshalb gut nachvollziehbar.
FAZIT
Genom-Editierung, eine neue Methode zur präzisen Modifikation von ausgewählten DNA-Bereichen bei Pflanzen oder Tieren, hat in den letzten Jahren große Aufmerksamkeit in der Züchtungsforschung - vor allem außerhalb Europas - erfahren. Die Hoffnung auf schnelle Zuchterfolge hat hier gleichzeitig dazu geführt, dass vermehrt öffentliche und/oder private Gelder in die Entwicklung von Genom-Editierungsorganismen fließen.
In der EU sind gentechnisch veränderte Organismen (GVO) seit langem Gegenstand hitziger Debatten, wobei sich die öffentliche Besorgnis oft nicht nur auf die Gesundheit und das Tierwohl beziehen, sondern auch mögliche Auswirkungen auf die Umwelt und die Verbrauchersicherheit einschließen.
Die aktuell gültige Entscheidung des Europäischen Gerichtshofs, dass mittels Genom-Editierung erzeugte Nutztiere genauso reguliert werden wie „klassische“ GVO, untermauert die restriktive Haltung gegenüber solchen Gentechnologien in der EU.
Deutschland gehört zu den Ländern, in denen die öffentliche Ablehnung dieser neuen Gentechnologie besonders ausgeprägt ist.
Wenn die Verbraucher die Produkte solcher Tiere hier weiter ablehnen, müssen die Rinderzüchter innerhalb der EU vorzugsweise an den konventionellen Zuchtmethoden festhalten.
In anderen Teilen der Welt wird man sicherlich Wege finden, auch die Genom-Editierung in Rinderzuchtprogrammen gezielt weiter zu integrieren.
DER DIREKTE DRAHT
Prof. Dr. habil. Wilfried Brade,
Professor für Tierzucht (i.R.) an der Tierärztliche Hochschule Hannover (TiHo),
aktuell: Norddeutsches Tierzucht-Beratungsbüro
E-Mail: wilfried.brade[at]t-online.de
Literatur – wird nicht gedruckt; steht auf Anfrage aber zur Verfügung
